بلومبرغ
في وقت من الأوقات تبدد الأمل وسادت حالة من الشك في لقاح أسترازينيكا نتيجة سلسلة الأخطاء غير المقصودة التي ارتكبتها شركة الأدوية البريطانية.
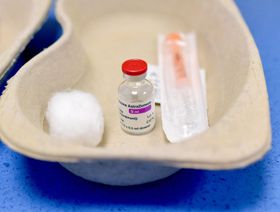
كانت ليلة الاثنين 22 مارس سعيدة بالنسبة لمين بانغالوس رئيس أبحاث المستحضرات الطبية الحيوية في "أسترازينيكا"AstraZeneca Plc حيث سيطر عليه الشعور بالرضا عن عمله لأول مرة منذ فترة بعد العمل على مدار الساعة خلال عطلة نهاية الأسبوع وحصوله للتو على نتائج مؤقتة تتفوق على تجارب وتوقعات اللقاحات الأمريكية، حيث أشارت النتائج إلى أن جرعة لقاح أسترازينيكا آمنة ومعدل فعاليتها 79% في منع حالات الإصابة بكوفيد 19 المصحوبة بأعراض.
أخيراً حصل بانغالوس على أخبار إيجابية بعد شهور من الترقب بشأن العديد من النقاط الهامة، بما في ذلك السلامة ونقص الإمدادات.
لم يهنأ بانغالوس طويلاً بحالة الرضا بعدما تلقى في سريره ببريطانيا مكالمة حوالي الساعة الخامسة من صباح اليوم التالي اهتز على أثرها بعدما سمع صوت باسكال سوريوت الرئيس التنفيذي لشركة أسترازينيكا يحدثه من أستراليا ليسأله ماذا يحدث عندك؟.
لقد أصدر المعهد الوطني الأمريكي للحساسية والأمراض المعدية (Niaid) للتو بياناً في وقت متأخر من الليل أعلن فيه أن مجلس مراقبة البيانات والسلامة DSMB الذي يشرف على تجارب اللقاح أبدى قلقه من إدراج أسترازينيكا معلومات قديمة خاصة بنتائج التجارب والتي "ربما تظهر بيانات ناقصة عن مدى فعالية التطعيم". وناشد المعهد الشركة نشر بيانات حديثة في أقرب وقت ممكن.
كما تلقى بانغالوس وفريق عمله في ساعة متأخرة أثناء نومهم في أوروبا بريداً إلكترونياً قاسياً من مجلس مراقبة البيانات والسلامة والذي يمثل لجنة خبراء مستقلة عينتها معاهد الصحة الوطنية الأمريكية للإشراف على التجارب السريرية اتهم فيه الشركة بنشر بيانات "تبدو مضللة" وأن البيانات كانت "أكثر ملاءمة للدراسة وليست البيانات الحديثة الكاملة". وذكر المعهد أن "مثل هذه القرارات تقوض ثقة الجمهور في مسار البحث العلمي".
تفاجأت الإدارة التنفيذية في أسترازينيكا بإسراع المعهد الوطني الأمريكي للحساسية والأمراض المعدية بنشر نقد اللجنة المستقلة للنتائج المؤقتة رغم عدم التواصل معهم لمناقشة المخاوف أولاً في واقعة غير مسبوقة في ذلك الشأن.
تسربت رسالة مجلس مراقبة البيانات والسلامة بسرعة إلى صحف واشنطن بوست ونيويورك تايمز. وفي غضون ساعات، ظهر أنتوني فاوتشي مدير المعهد الوطني للحساسية والأمراض المعدية في برنامج "صباح الخير أمريكا" يتحدث عن الإخفاق وقال: "من المؤسف حقاً أن يحدث هذا". وأضاف: "هذا ما يمكن تسميته خطأ غير مقصود، وهناك احتمال كبير أن يكون اللقاح جيد جداً، لأن ذلك الخطأ غير مؤثر لكنه يثير الشكوك".
كانت أسترازينيكا قد تلقت موافقة مجلس السلامة على إجراء التحليل المؤقت بناءً على نتائج 141 حالة كوفيد 19 تم التحقق منها بتاريخ 17 فبراير. وأوصى المجلس فريق أسترازينيكا بالأخذ في الاعتبار الحالات التي لم يتم التحقق منها والتي ظهرت منذ ذلك الحين للتأكد من عدم تحديد نسبة فعالية تختلف بشكل كبير عن النتائج الفعلية وفقاً لمصادر مطلعة على المناقشات. لكن فريق العمل قام بمراجعة الحالات ووجد أن تأثيرها المحتمل على نسب الفعالية ضئيل، لذلك لم يذكروا في بيانهم أن النسبة النهائية قد تتغير.
نتائج محدثة عن اللقاح
سارع الفريق المشرف على التجارب بعد إعلان مجلس مراقبة البيانات والسلامة النتائج للجمهور إلى مراجعة 49 حالة إضافية في عملية تستغرق أسابيع في الظروف العادية. لكن أسترازينيكا أعلنت بعد يومين عن نتائج محدثة وكانت الفروق غير ذات دلالة إحصائيا، حيث انخفض مستوى الفعالية الإجمالية 3 نقاط مئوية إلى 76% على الرغم من ارتفاع النتائج الفعلية لكبار السن لتصل 5 نقاط مئوية إلى 85%. كما أظهر اللقاح فعالية بنسبة 100% في الوقاية من الإصابة بأعراض شديدة والحاجة لدخول المستشفى لتلقي العلاج.
كانت استرازينيكا حريصة هذه المرة على تأكيد ملاحظة استمرار وجود 14 حالة أخرى تحتمل إصابتها بكوفيد 19 ويجري تقييمها وهو ما قد يتسبب في تغير المؤشرات. وأبدى المسؤولون التنفيذيون في الشركة انزعاجهم بشدة مما حدث خلال الأسبوع. حيث قال أحدهم: "إنه أمر محبط للغاية". وأضاف: "بصراحة هذا يكسر قلوبنا".
بعد أسبوع من ظهور النتائج المحدثة عقب فاوتشي مستنكراً التصعيد الدرامي الذي حدث عندما قال رداً على سؤال من قبل بلومبرغ بيزنس ويك في خطاب دوري بالبيت الأبيض يوم 31 مارس: "لم أشكك في بياناتهم على الإطلاق". وأضاف فاوتشي "إنه لقاح جيد سيكون له دور مهم للغاية في الاستجابة العالمية للجائحة".
تعرض اللقاح الذي طورته أسترازينيكا بالتعاون مع جامعة أكسفورد إلى تغيرات دراماتيكية شملت نوايا طيبة وأخطاء في التواصل وفوضى بالتجارب وكوابيس بشأن التصنيع والتنافس السياسي والاقتصادي. والأخطر مما سبق اتهام العديد من التقارير اللقاح بتسببه في إصابة عدد قليل من الأشخاص الذين تلقوه، ومعظمهم تقل أعمارهم عن 60 عاماً، بنوع نادر من تخثر الدم في المخ.
وأكدت منظمة الصحة العالمية والجهات التنظيمية البريطانية والأوروبية وجود صلة محتملة بين اللقاح والجلطات، لكنها أشارت إلى أن فوائد الحصول على اللقاح تفوق المخاطر.
وأوصت الجهات التنظيمية في الاتحاد الأوروبي بإدراج التخثر كأثر جانبي نادر، بينما أوصت بريطانيا بعدم استخدام الأشخاص الذين تقل أعمارهم عن 30 عاماً لقاح أسترازينيكا. وقد أوقفت بعض الحكومات بالفعل استخدام اللقاح بالنسبة للأشخاص الأصغر سناً.
ولكن وعلى الرغم من تلك المشكلات، طالب العديد من قادة الاتحاد الأوروبي باستلام جرعات أسترازينيكا وقدموا شكاوى ضد الشركة يتهموها بالفشل في الوفاء بوعودها بشأن الإمدادات وبلغ الأمر التهديد بمنع تصدير اللقاحات المصنوعة أو المعبأة داخل دول الاتحاد الأوروبي.
تحول درامي شهده لقاح أسترازينيكا في غضون عام تحول على أثرها من أفضل منتجات عائلة لقاحات فيروس كورونا إلى المعاناة الشديدة من العديد من المشاكل.
قبول الآثار الجانبية
يقول جون بيل أستاذ الطب في أكسفورد المولود في كندا والمشرف على التواصل بين الجامعة وأسترازينيكا: "إنها السحابة الصغيرة التي تتبعك في كل مكان تذهب إليه وأعتقد أنها غير عادلة إلى حد ما". وأضاف بيل: "إذا استمر الناس في العزوف عن اللقاح فلن يثق أحد بعد ذلك في استخدام دواء له آثار جانبية وستصبح هناك مشكلة كبيرة، وخاصة أن اللقاح سهل التوزيع ورخيص ويمكن استخدامه عالمياً كما يبدو أنه فعال للغاية".
وأشار بيل إلى سهولة نقل وتخزين لقاح أسترازينيكا بشكل أفضل من اللقاحات القائمة على تقنية mRNA والتي تنتجها مودرنا وفايزر-بايونتيك.
وتعهدت الشركة البريطانية بتقديم نحو 3 مليارات جرعة خلال 2021 وبيعها على أساس غير هادف للربح مقابل دولارات معدودة. وذلك في الوقت الذي يتوقع فيه أن تقدم جونسون أند جونسون لقاحا بجرعة واحدة وقد وافقت الشركة أيضاً على بيعه بدون ربح في إطار مساهمتها في إنهاء الوباء لكن لقاح جونسون أند جونسون تأخر كثيراً في الإنتاج مقارنة بلقاح أسترازينيكا.
على النقيض من ذلك، تتوقع فايزر تحقيق إيرادات تصل إلى 15 مليار دولار هذا العام من بيع لقاح فايزر-بايونتيك، كما تتوقع موديرنا إيرادات بقيمة 18 مليار دولار من بيع لقاحها.
تم حتى أبريل توزيع أكثر من 135 مليون جرعة من لقاح أسترازينيكا في جميع أنحاء العالم، وأصبحت جرعات اللقاح تمثل العمود الفقري لبرنامج كوفاكس الذي تدعمه منظمة الصحة العالمية بهدف توفير اللقاحات للبلدان المنخفضة والمتوسطة الدخل.
صادف الحظ السيئ كلا من أسترازينيكا وأكسفورد. لكن ذلك لا ينفي عنهما ارتكاب سلسلة من الأخطاء التي أبعدتهما عن المكانة التي يستحقانها في مقدمة الشركات المنتجة للقاح.
ضغوط العمل في تطوير اللقاح
يقول حزقيال إيمانويل أستاذ الأخلاقيات الطبية والسياسة الصحية في جامعة بنسلفانيا والذي قدم استشارات لفريق الرئيس بايدن الانتقالي بشأن مكافحة كوفيد: "أمر مروع أن نرى ارتكابهم الكثير من الأخطاء". وأشار إيمانويل إلى الحاجة الماسة لدى العالم للحصول على لقاح أسترازينيكا لإنهاء الوباء على الرغم من كل تلك الأخطاء الفادحة. وأضاف ايمانويل، هكذا سارت الأمور على نحو خاطئ وقال: "يجب أن نكون قادرين على الوثوق في اللقاحات. كما لا يمكننا تجاهل تلك النتائج".
أحرز علماء أكسفورد تقدما سريعا في الاختبارات المعملية والحيوانية للقاح أسترازينيكا خلال الربيع الماضي، وقد خططوا لتقديمه عن طريق جرعة واحدة في ذلك الوقت. كما تعرضوا لضغط العمل مع شركة أدوية كبيرة تحتاج إلى شهور لاستكمال عملية التصنيع على نطاق واسع وما تحتاجه من تخطيط مكثف وقدرة لوجستية هائلة لنقل وتوزيع اللقاح.
أوقفت شركة ميرك أند كو الأمريكية محادثاتها المبكرة بعد ما أبدى مسؤولون بريطانيون قلقهم حيال تصعيد أمريكي قد يمنعهم من الحصول على جرعات اللقاح ورأوا ضرورة إبقاء التطوير والتصنيع في أيدي البريطانيين. وكانت جلاكسو سميثكلاين والتي تعد شركة تطوير لقاحات رئيسية في بريطانيا من بين الشركات التي تحظى بفرصة للتعاون مع الجامعة لكنها لم تكمل محادثاتها. لتبقى شركة أسترازينيكا الوحيدة بين الشركات البريطانية القادرة على التعاقد مع الجامعة.
قاد باسكال سوريوت أسترازينيكا 2014 حينما رفضت عرض استحواذ بقيمة 117 مليار دولار من شركة فايزر ونجح سوريوت في تحسين سمعة الشركة لتشتهر بكونها منتج الأدوية الجديدة التي تحمل معجزات وخاصة أدوية علاج السرطان.
وقال جون بيل في أبريل الماضي إن أكسفورد لديها شرطين لإتمام التعاقد: الأول، ضرورة بيع اللقاح على أساس غير هادف للربح على الأقل للسنة الأولى، والثاني، مساعدة أسترازينيكا لدول العالم النامي في الحصول على الجرعات. وأكد بيل أن سوريوت لم يتردد في الموافقة وأجاب: "أنا معك تماماً". حيث أكد سوريوت أن أسترازينيكا سوف تبني علاقات متميزة تمكنها في المستقبل من توسع أعمالها إذا ثبتت ضرورة الحصول على جرعات معززة أو سنوية.
تفتقد أسترازينيكا لخبرة تطوير اللقاحات، حيث تقتصر خبرتها في ذلك الشأن على بخاخ أنف للإنفلونزا. وقد ذكر بيل ذلك قائلاً: "يدخلون هذه اللعبة للمرة الأولى فهم يشقون طريقهم في هذا الشأن". وأضاف: "ليس لديهم قوة تأثير أو شخصيات موثوقة في عالم اللقاحات للوقوف والقول مرحباً يا رفاق انتبهوا إلى ما نقدمه فهو حقاً لقاح جيد".
تجارب وبروتوكولات
منذ بداية مراحل تجربة اللقاح كان واضحاً احتمال حدوث خلل وظيفي في مسار الوصول للقاح نهائي. حيث توصلت أسترازينيكا إلى اتفاقية شراكة نهائية مع أكسفورد بحلول نهاية أبريل بينما كانت الجامعة قد بدأت بالفعل التجارب البشرية والتي عادة ما تشهد بروتوكولاتها تعقيدات شديدة. وكان من المقرر أن تبدأ تجارب المرحلة الثالثة الواسعة في بريطانيا والبرازيل إلى جانب المرحلة الأولى والثانية الأصغر في جنوب أفريقيا. وفيما يخص الجزء الخاص بالمرحلة الثالثة والمقرر إجراؤه في الولايات المتحدة فقد تولت أسترازينيكا المسؤولية وتم الاتفاق وتصميم بروتوكول مباشر بين الشركة والجامعة.
تحركت الشراكة بسرعة نحو التصنيع وإطلاق الإنتاج محلياً بدعم من الحكومة البريطانية واستناداً إلى العمل المبكر للجامعة مع أكسفورد بايوميديكا Oxford Biomedica الشركة الصغيرة التي تركز أعمالها على التكنولوجيا الحيوية. حيث أعلنت الحكومة البريطانية في منتصف مايو طلبها المسبق لتأمين 100 مليون جرعة مقابل تعهدها بدعم عمليات سرعة الإنتاج الفائقة، إضافة إلى برنامج الرئيس السابق دونالد ترمب بقيمة 1.2 مليار دولار والذي يهدف إلى تسريع الحصول على اللقاح مقابل تأمين 300 مليون جرعة للولايات المتحدة.
ومع بدء أكسفورد مرحلتها الثالثة مبكراً في بريطانيا بدا أن كل شيء يقترب.
رغم كل تلك المؤشرات الإيجابية، أدرك علماء أكسفورد الذين يعملون بعيداً عن الأنظار خطأهم في تقدير مدى تركيز اللقاح وبالفعل بدأوا في تقديم نصف جرعة لبعض المشاركين في المرحلة الثالثة كما قرر فريق العمل في نفس الوقت تقريباً الانتقال لنظام الجرعتين بدلاً من الواحدة بعد ظهور مؤشرات أن نظام الجرعتين سيؤدي إلى تحقيق حماية أفضل مع الاتفاق أن تكون الفترة بين الجرعتين نحو أربعة أسابيع.
بالفعل حصلوا على موافقة الجهات التنظيمية البريطانية بالمضي قدماً وتم تقديم نصف جرعة للمتطوعين على أن تتبعها جرعة ثانية، ولكن سوء التقدير وقرار تقديم جرعة ثانية احتاج من فريق التصنيع وقتا إضافيا لإنتاج مزيد من اللقاحات، الأمر الذي أدى إلى تأخير الجرعة الثانية لعدد كبير من المتطوعين.
برر فريق العمل والجهات التنظيمية الاستمرار في تقديم نصف جرعة تحت ضغوط تسارع تفشي الوباء واشتداد الحاجة للتوصل إلى لقاح ما اضطرهم إلى مخالفة قواعد العمل في الظروف الطبيعية التي تقضي تجربة أنظمة جرعات مختلفة. وهو ما أثار تحفظ بعض المسؤولين الأمريكيين عند علمهم بتلك التغييرات على البروتوكول وسيطر عليهم تساؤل: "ماذا يفعل هؤلاء الرجال؟" وفقاً لشخصية بارزة سابقة في إدارة ترمب. وهو ما أثر على ثقة الجهات التنظيمية الأمريكية في المطورين البريطانيين وتزامن ذلك في نفس الوقت الذي تعمل فيه معاهد الصحة الوطنية الأمريكية Niaid مع أسترازينيكا لإعداد تجارب المرحلة الثالثة في الولايات المتحدة.
كان فريق عمل أسترازينيكا يأمل بدء تجارب المرحلة الثالثة في الولايات المتحدة الأمريكية في يوليو، لكن الأمر انتهى إلى بدئها بالتزامن مع بدء شركتي موديرنا وفايزر نفس المرحلة. نتيجة مطالبة المسؤولين الأمريكيين التأكد من إمكانية توسعة نطاق تصنيع اللقاح واختباره قبل بدء تجارب المرحلة الثالثة باهظة الثمن وهو ما استغرق وقتاً أطول من المتوقع وفقا لثلاثة مسؤولين كبار سابقين. كما طالبت إدارة الغذاء والدواء الأمريكية وبعض مسؤولي برنامج تسريع اللقاح بالحصول على بيانات استجابة مناعية مفصلة لمتطوعين تزيد أعمارهم عن 65 عاماً بحسب ما ذكرت مصادر مطلعة والتي أكدت أن استجابة أكسفورد كانت بطيئة بسبب صعوبة الحصول على متطوعين كبار السن في تجربتها الواسعة في بريطانيا.
أدت تلك العوامل إلى عدم تمكن أسترازينيكا من بدء تقديم جرعات للمتطوعين في الولايات المتحدة حتى نهاية شهر أغسطس.
بعد أسبوع فقط من بدء تجارب المرحلة الثالثة، ذكرت خدمة ستيت الإخبارية Stat توقف تجارب المرحلة الثالثة في الولايات المتحدة مؤقتاً بعد معاناة أحد المتطوعين في بريطانيا من مرض غير معروف، ما أدى إلى تعليق التطعيم في جميع التجارب العالمية التي تشرف عليها الشركة حتى يتم التحقيق. ومن الطبيعي أن يتم إيقاف التجارب السريرية كإجراء احترازي، وخاصة في المراحل النهائية التي عادة ما تكون واسعة النطاق ويصبح ذلك التوقف تأكيدا على حرص القائمين على التجارب على السلامة. لكنها بطبيعة الحال ليست تجارب عادية. إنها أكثر المشاريع العلمية على مدار التاريخ التي تحظى بمراقبة العالم عن كثب.
رغم ذلك أثار أول توقف لتجارب لقاح فيروس كورونا عاصفة إعلامية.
ضغوط الإفصاح
عادة ما تمر تلك الملاحظات دون أن يلحظها أحد، لكن كان هناك ضغوط كبيرة للإفصاح عن مزيد من التفاصيل، وهو ما رفضه فريق العمل وأرجعوا ذلك للحفاظ على سرية بيانات المشاركين في التجارب، وهي ممارسة متعارف عليها في مثل تلك الأحداث. ونتيجة لتلك الضغوط أعلن مات هانكوك وزير الصحة البريطاني توقف تجارب المرحلة الثالثة التي تجريها أكسفورد بشكل مؤقت نتيجة مخاوف تتعلق بالسلامة.
لكن سوريوت كشف فيما بعد خلال اتصال هاتفي مع مستثمر خاص عن بعض التفاصيل التي طالب بها الصحفيون والعلماء. حيث أشار إلى أن ما تعرض له أحد المشاركين، وكانت امرأة يتمثل في أعراض عصبية تبدوا كأعراض التهاب النخاع الشوكي الذي يمكن أن تتسبب فيه عدوى فيروسية. وقال سوريوت إنه من غير الواضح ما إذا كان قد تم تشخيص هذه الحالة المحددة، وإن كان السبب فيها هو اللقاح. ولكن بمجرد أن تسربت المعلومات عادت العاصفة إلى السطح مرة أخرى.
تسببت تصريحات سوريوت الانتقائية عن حالة المرأة في تجدد المطالب بالحصول على مزيد من التفاصيل وهو ما رفضته الشركة، بالإضافة إلى شكوى المرأة التي تم تناول حالتها الصحية في كافة وسائل الإعلام بجميع أنحاء العالم وفقاً لمصادر مطلعة على الأحداث. حيث يهدد الإفصاح عن معلومات إضافية حول حالتها قبل إجراء تحقيق كامل إلى التشكيك بمدى نزاهة التجارب كما قد يشجع مشاركين آخرين على الإعلان عن تعرضهم لمشكلات مماثلة دون أن يتم التحقق بشأنها.
عادت التجارب مرة أخرى بعد أسبوع من التوقف المؤقت بعدما سمحت باستئنافها الجهات التنظيمية في البرازيل وبريطانيا، لكن الولايات المتحدة أبقت التجارب معطلة لسبعة أسابيع تقريباً، وهو ما سمح لشركتي فايزر وموديرنا الإسراع بتجاربهم للحاق باسترازينيكا.
طلب المسؤولون الأمريكيون من أسترازينيكا معلومات تفصيلية عن أية أعراض عصبية لكافة المشاركين في التجارب الذين تلقوا اللقاح وفقاً لمصادر مطلعة على طلب السلطات الأمريكية. وقال ثلاثة من كبار المسؤولين الأمريكيين السابقين إنهم شعروا بالإحباط بسبب المدة التي استغرقتها أسترازينيكا لتزويدهم بالبيانات التي طلبوها. بينما قال مسؤول سابق، إن إدارة الغذاء والدواء لم تكن لديها رغبة في تعطيل التجارب في ظل الحاجة الملحة للوصول للقاح وسط سرعة تفشي الوباء.
اعتقد العديد من المسؤولين الأمريكيين أن أسترازينيكا وأكسفورد لديهما مشكلات في التواصل، ما تسبب في تأخير تقديم البيانات بالمقارنة بالشركات الأخرى التي استجابت بسرعة لطلبات إدارة الغذاء والدواء الأمريكية. كذلك أبدى بعض العاملين ببرنامج الحكومة البريطانية للإسراع باللقاح انزعاجهم من تعطل التجارب.
تعثر لقاح جونسون
أعلنت خدمةStat الإخبارية في 12 أكتوبر، توقف تجارب شركة جونسون أند جونسون بشكل مؤقت نتيجة ظهور مرض غير معروف. ولم تعلن الشركة الأمريكية عن التوقف ورفضت الكشف عن التفاصيل حفاظاً على خصوصية المريض كما فعلت أسترازينيكا، لكنها كشفت لاحقاً في تقرير قدمته جونسون أند جونسون إلى إدارة الغذاء والدواء الأمريكية أن تفاصيل المرض تعود إلى معاناة متطوع يبلغ من العمر 25 عاماً من تخثر الدم في المخ مما أدى إلى نزيف دماغي.
استأنفت جونسون أند جونسون تجاربها في الولايات المتحدة بعد التأكد أن المرض لم يكن له علاقة باللقاح وقالت إنها سوف تستأنف التجارب مرة أخرى بعد أقل من أسبوعين من التوقف.
أثارت تلك الأحداث الشك لدى بعض المسؤولين الأمريكيين بشأن ما إذا كان لقاح أسترازينيكا آمناً، وتزامن ذلك مع اقتراب توصل فايزر وموديرنا للقاح وإسراع جونسون أند جونسون في تجاربها.
يقول مسؤول سابق في إدارة ترمب: "بدت أسترازينيكا مثل تشكيل عصابي لا يستطيع إطلاق النار". وأضاف: "موقف الشركة أصبح يتوقف على قرارهم حول ما إذا أرادوا أن يفعلوا ذلك أم لا، ولن نبذل جهدا إضافيا كي ينجح لقاح أسترازينيكا فقد حصلوا على العديد من الفرص".
بحلول نوفمبر، كانت نتائج تجارب شركتي فايزر وموديرنا قد توصلت إلى أن فعالية لقاحاتهم فاقت توقعات الجميع واقتربت من 95% وبعدها بأيام قليلة وتحديداً في 23 نوفمبر، أعلنت أكسفورد التوصل لنتائج مؤقتة جيدة لتجاربها في بريطانيا والبرازيل، لكنها تبدو فوضوية بالمقارنة بنتائج فايزر وموديرنا.
أبلغت فايزر عن بيانات فعالة لأكثر من 40 ألف مشارك في التجارب، وسجلت موديرنا أكثر من 30 ألف مشارك، بينما سجلت أكسفورد أقل من 12 ألف مشارك. كما لم تعلن أكسفورد عن رقم محدد وواضح لنسبة الفعالية، بل أعلنت نسبتين وهو ما يرجع إلى إعطاء مجموعة من المشاركين نصف جرعة في المرة الأولى. أما بالنسبة لمجموعة المشاركين الذين حصلوا على جرعتين متباعدتين على مدار شهر تقريباً فقد بلغت نسبة فعالية اللقاح 62%. بينما المجموعة الأصغر والمكونة من حوالي 2700 مشارك وهي المجموعة التي تلقت جرعة في المرة الأولى ارتفعت نسبة فعالية اللقاح عندها إلى 90%.
تضاربت الروايات التي سردتها كل من أكسفورد وأسترازينيكا بشأن فعالية الجرعات وما حدث مع مجموعتي التجارب. حيث قالت سارة غيلبرت عالمة أكسفورد التي قادت عملية تطوير اللقاح، أن الأمر يبدو طبيعياً في التجارب، وقالت لبلومبرغ نيوز: "لا نريد التمسك بنتائج جرعة منخفضة للغاية ثم نكتشف أن الاستجابة المناعية منخفضة للغاية أيضاً". وأضافت غيلبرت: "نسعى إلى الحصول على نظام تطعيم جيد وفعال".
في اليوم التالي قال بانغالوس لرويترز، إن علماء أكسفورد "قللوا من توقعاتهم بشأن فعالية الجرعة بمقدار النصف". ووصف النجاح النسبي للجرعة القليلة على أنه "صدفة".
وتأثرت نتيجة فعالية المجموعة الأصغر بالمشهد المتداخل من النتائج غير الدقيقة للتجارب إلى جانب عدم قدرة أكسفورد وأسترازينيكا على التنسيق فيما بينهما وتقديم رواية واحدة تفسر ما حدث. حيث يقول أحد كبار المسؤولين البريطانيين السابقين: "لم تكن أفضل أوقاتهم".
لم يظهر التوتر على العلاقات بين أسترازينيكا وأكسفورد رغم تلك الأحداث. لكن التصريحات التي لازمت الطرفين تظهر إلقاء كل منها اللوم على الآخر. فعندما يتحدث المسؤولون التنفيذيون في أسترازينيكا عن التجارب في بريطانيا كانوا يقولون: "إنها تجربة أكسفورد ولا علاقة لنا بها". وفي المقابل وعند سؤال علماء أكسفورد عن سبب تأخر التجارب في الولايات المتحدة يقولون: "إنها تجربة أسترازينيكا ولا علاقة لنا بها".
أكد بيل أن العلاقة جيدة وقال: "ما زلنا نحاول مساعدة أسترازينيكا. لقد ارتبطنا بهم من البداية".
أعلنت الجهات التنظيمية البريطانية في 30 ديسمبر صلاحية لقاح أكسفورد مع التوصية بفاصل زمني 12 أسبوعاً بين الجرعتين بعدما خلص الخبراء البريطانيون إلى أن الفعالية الأعلى للمشاركين الذين تلقوا نصف الكمية في الجرعة الأولى ترجع على الأرجح إلى الفاصل الزمني الكبير بين الجرعتين ولا علاقة له بكمية الجرعة الأولى.
بدء الإنتاج
بدأ الإنتاج بالفعل في عدة مواقع داخل بريطانيا في ذلك الوقت. وأصبحت بريطانيا على استعداد للتوسع في توفير اللقاحات من 4 يناير أي بعد مرور نحو شهر على إطلاق البرنامج الوطني للتطعيم الذي بدأ بالجرعة الأولى من لقاح فايزر – بايونتيك.
عملت أكسفورد بيوميديكا على مدار أشهر لعلاج نقاط الضعف في عملية تصنيع لقاح أسترازينيكا ومحاولة التغلب على مشاكل الإنتاج الكبيرة، وزيادة بنوك الخلايا التي من شأنها أن تثبت قدرتها على إنتاج مليوني جرعة أسبوعياً. وبحلول الربيع، استحوذت لقاحات أسترازينيكا على أكثر من نصف الجرعات التي يتم تناولها في بريطانيا، كما أظهرت البيانات انخفاض أعداد الوفيات والحالات التي تحتاج إلى رعاية صحية داخل المستشفيات.
الوضع بدا مختلفاً في أماكن أخرى داخل القارة الأوروبية والتي شهدت وتيرة تلقيح أبطأ بكثير من بريطانيا. حيث أعلنت أسترازينيكا في نهاية يناير، وقبل أيام قليلة من حصولها على موافقة وكالة الأدوية الأوروبية على اللقاح، عن قدرتها على تسليم 31 مليون جرعة فقط لدول الاتحاد الأوروبي خلال الربع الأول بدلاً من وعودها السابقة بتسليم 120 مليون جرعة خلال تلك الفترة.
لم يكن الاتحاد الأوروبي قد وقع عقدا مع الشركة بعد ولكنه اتفق معها على أن يحصل على 400 مليون جرعة حتى نهاية أغسطس، وهو ما يضع الإنتاج داخل القارة خلف بريطانيا بأشهر. كما جاء إنتاج المصنع البلجيكي المتعاقد على تصنيع لقاحات أسترازينيكا أقل من المتوقع، في الوقت الذي لم يكن المصنع الهولندي قد حصل على موافقة وكالة الأدوية الأوروبية حتى نهاية شهر مارس.
بدا الغضب واضحاً على المسؤولين في بروكسل بسبب نقص الإمدادات. وحاول تييري بريتون رجل الأعمال السابق الذي يشغل منصب مفوض السوق الداخلية في الاتحاد الأوروبي إقناع زميله الفرنسي سوريوت بتعزيز عمليات التسليم، ولكن دون جدوى.
ازداد الأمر سوءاً بسبب عدم تواجد سوريوت في أوروبا حيث كان يعمل من سيدني مقر إقامة عائلته من قبل حلول عيد الميلاد. وظهر ذلك جلياً عندما قال بريتون لمحطة أوروبا 1 الإذاعية الفرنسية في 14 مارس أنه يستيقظ كل يوم الساعة 4:30 صباحاً للاتصال بسوريوت. حيث قال: "لا أقصد توجيه الانتقاد ولكن على كل واحد منا بذل أقصى ما في وسعه وتدبير أموره". وأضاف: "كما ترى يتطلب الأمر مني زيارة مصنعين أو ثلاثة من مصانع الشركة أسبوعياً. وأنا لا أدعي معرفة مصانعهم أكثر منهم ولكني أريد أن أكون في موقع العمل".
قالت أسترازينيكا إن سوريوت يعمل على مدار الساعة من أستراليا.
الأطماع في اللقاحات
بحلول منتصف مارس عادت رئيسة المفوضية الأوروبية أورسولا فون ديرلاين للتهديد بحظر تصدير جميع اللقاحات التي يتم تصنيعها داخل الاتحاد الأوروبي. وازداد جنون المشهد بعد بضعة أيام مع سحب أسترازينيكا لجرعات متوجهة لأوروبا وتحويلها إلى بريطانيا، وهو ما تزامن مع إصدار بروكسل توجيهاتها للقادة الإيطاليين بمداهمة الشرطة لمصنع تعبئة عبوات لقاح أسترازينيكا في مدينة أنغاني والذي كان يحتوي على 29 مليون جرعة، ولكن تبين بعد ذلك أن الجرعات تمثل مخزونا متجها إلى أوروبا وبرنامج كوفاكس.
ورغم أن العديد من القادة الأوروبيين أعربوا عن مخاوفهم بشأن فعالية وسلامة اللقاح، إلا أن الطلب الكثيف استمر على الإمدادات في ظل حظر 10 دول أوروبية على الأقل استخدام اللقاح لمن هم أكثر من 65 عاماً أوائل فبراير في ظل عدم توفير أكسفورد بيانات لتلك الفئة العمرية ضمن نتائج تجارب المرحلة الثالثة.
تدفقت الأخبار السلبية، حيث أظهرت تجربة أكسفورد أن اللقاح يوفر الحد الأدنى للحماية من فيروس جنوب أفريقيا المتحور، وتبع ذلك إعلان الدنمارك والنرويج وأيسلندا منتصف مارس تعليقا مؤقتا لجرعة أسترازينيكا حتى يتم التحقيق في ظهور مرض نادر من تخثر الدم تم اكتشافه لدى العديد من الذين تلقوا التطعيم ونتجت عنه وفاة أحدهم على الأقل.
أوقفت ألمانيا بعد أيام استخدام اللقاح وتبعها العديد من الدول الأوروبية رغم توصية وكالة الأدوية الأوروبية باستمرار تلقي اللقاح بعد مراجعة الوكالة البيانات وتأكيدها أن فوائد الجرعة تفوق بكثير المخاطر.
تخثر الدم
تم استئناف الاستخدام مرة أخرى ولم يمض وقت طويل حتى تم اكتشاف المزيد من الحالات. وبنهاية مارس، أوقفت كندا استخدام لقاح أسترازينيكيا لمن يبلغ من العمر 55 عاماً أو أقل، كما أعادت ألمانيا تعليق استخدامه لمن هم أقل من 60 عاما.
علقت المستشارة الألمانية أنغيلا ميركل، وهي يبدو على ملامحها الإرهاق أثناء حديثها، قائلة: "يجب أن نكون قادرين على الوثوق في اللقاحات". وأضافت: "هذه النتائج لا يمكننا تجاهلها" في إشارة إلى 31 شخصا أصيبوا بأحد أشكال تخثر الدم في ألمانيا والمعروف باسم تجلط الجيوب الوريدية الدماغية (CVST)، والذي تم الإبلاغ عنه من بين حوالي 2.7 مليون جرعة تم تناولها وهو ما يعد معدل إصابة يفوق المعدل الطبيعي.
كانت بعض الحالات مصحوبة بانخفاض مستويات الصفائح الدموية وكان أغلبهم من النساء الأصغر سنا ومتوسطات العمر. وتوفي منهم تسع حالات.
شمل التحقيق الذي قامت به وكالة الأدوية الأوروبية حتى 22 مارس تعرض 86 حالة من بين 25 مليون شخص تلقوا اللقاح داخل أوروبا وأماكن أخرى للإصابة بتخثر الدم توفيت على أثرها 18 حالة ثم زادت الإصابات حتى بلغت 222 حالة بحلول 7 أبريل، وجاء تشخيصها بأنها تعاني من تخثر الدم في المخ والبطن. وأعلنت الوكالة أن بيانات المرضى لا تشير إلى سبب محدد أو تاريخ مرضي محدد للحالات.
علق إمير كووك المدير التنفيذي لوكالة الأدوية الأوروبية قائلاً: "من الواضح أن تلك الإصابات أحد التحديات التي تفرضها حملات التطعيم واسعة النطاق". وأضاف كووك: "عندما يتلقى ملايين الأشخاص اللقاحات، يمكن أن تحدث إصابات نادرة جداً لم يتم تحديدها أثناء التجارب السريرية".
وقالت الجهات التنظيمية البريطانية إن معدل الإصابة بالجلطات الدماغية بلغ حوالي 4 حالات لكل مليون شخص تلقوا اللقاح. فيما أعلنت وكالة الأدوية الأوروبية أن نسبة المخاطر بالإصابة بتخثر الدم داخل أوروبا تبلغ 1 من كل 100 ألف شخص يتلقى اللقاح.
تفاوت الأعراض الجانبية
قد يرجع انخفاض عدد الإصابات في بريطانيا مقارنة بباقي أنحاء أوروبا إلى عدم البدء في تطعيم من هم تحت سن الخمسين، على الرغم من أن وكالة الأدوية الأوروبية قالت إنه لا يوجد دليل على أن الجلطات مرتبطة بالعمر أو الجنس.
تقدر كلية الطب بجامعة جونز هوبكنز احتمال الإصابة بتجلط الجيوب الوريدية الدماغية أن يكون لكل حالة من بين 200 شخص من جميع الأعمار يطورون CVST في سنة معينة.
أصدرت أسترازينيكا بياناً صحفياً في 7 أبريل استجابة للنتائج التي توصلت إليها الجهات التنظيمية وأكدت أنها ستجري تغييرات بحسب توصيات تلك الجهات تضع فيها تحذيراً على ملصق اللقاح كما أنها "تعمل بالفعل على مراجعة تلك الحالات الفردية ومحاولة فهم الأسباب التي تفسر تلك الإصابات النادرة للغاية".
ادى تسريب تقرير مجلس السلامة الأمريكي إلى تبدد آمال الإدارة التنفيذية في أسترازينيكا بشأن إمكانية تقدم نتائج تجربتهم الأمريكية الأكبر والأكثر قوة ما يدعم أمان وفعالية لقاحهم.
الإعلان عن بيانات مؤقتة يمثل مخاطرة في علم الأوبئة. لكن أسترازينيكا تعرضت لضغوط كبيرة من الجهات التنظيمية الأوروبية التي طالبتها بمزيد من البيانات والشفافية حول فعالية اللقاح على كبار السن واحتمال التعرض لتخثر الدم. وذلك في الوقت الذي تدرك فيه الإدارة التنفيذية جيداً خطورة التباطؤ في تقديم البيانات كما أن طبيعة أسترازينيكا كشركة مساهمة عامة يلزمها بالإفصاح عن التطورات بشكل سريع. وقد تعرضت الإدارة التنفيذية في الشركة يوم 21 مارس لحادثة أثرت نفسيا عليهم قبل يوم واحد من الإعلان عن النتائج المؤقتة بعدما علموا بوفاة خوسيه باسيلغا رئيس أبحاث الأورام في الشركة بشكل مفاجئ.
وفي اليوم نفسه، أجرت أسترازينيكا مع بعض المسؤولين الأمريكيين، ومن بينهم فاوتشي ومدير المعاهد الصحية الوطنية فرانسيس كولينز ومسؤولون أمريكيون آخرون فيما لم يحضر أحد من مجلس مراقبة البيانات والسلامة، مكالمة عبر الفيديو قدمت الشركة خلالها نتائج ضمت حالات إضافية غير مؤكدة، وأشارت إلى أن معدل الفعالية النهائي قد ينخفض بضع نقاط مئوية، لكنه سيرتفع بالنسبة لكبار السن، بينما لم يعترض أي من الحاضرين وفقاً لمصادر مطلعة على المناقشات.
وفي يوم الاثنين التالي أعلن بانغالوس النتائج المؤقتة وأشار إلى أن حالات إضافية قد ظهرت، بينما لم تعرض أسترازينيكا في بيانها كيفية تأثير تلك الحالات على معدل الفعالية الخاص باللقاح وهو ما أظهر تناقضاً صارخاً مع ما فعلته كل من فايزر ومودرنا قبل أشهر.
المنافسة تحتدم
زادت فايزر معدل فعاليتها من تقديراتها الأولية البالغة 90% لتصل إلى 95% بعد أسبوعين ما يمثل تفوقاً واضحاً على مستوى الفعالية والسمعة أيضاً. على النقيض أعلن مجلس مراقبة السلامة والبيانات الأمريكي احتمال تراجع معدل فعالية لقاح أسترازينيكا إلى ما بين 69 -74% بمجرد التحقق من صحة جميع الحالات وهي التقديرات التي لم يقدمها المجلس للشركة إلا بعد الإعلان عنها بشكل علني.
لم يكن ما قام به مجلس مراقبة السلامة والبيانات الأمريكي أمراً عادياً. فبينما يكون المجلس مسؤولاً بشكل أساسي عن مراجعة بيانات السلامة وتحديد متى تحقق التجربة حداً للفعالية تكون مسؤولية تحديد معدلات الفعالية النهائية من اختصاص هيئة إحصائية مستقلة تتعاون مع الشركة بشروط متفق عليها مسبقاً، وفي حالة وجود خلافات بعد مراجعة المجلس للبيانات يتم مراجعتها مع الشركة ومناقشة وجهات النظر خلف الأبواب المغلقة.
أشارت بولي روي أستاذة علم الفيروسات في كلية لندن للصحة وطب المناطق الحارة، إلى أهمية الدقة بشكل كبير بالنسبة لأسترازينيكا وخاصة في مثل تلك الحالات حيث قالت: "ما كان يجب أن يعلنوا رقماً معيناً إذا لم يكونوا متأكدين". وأضافت روي: "لا مشاكل بشأن اللقاح نفسه، ولكن المشكلة في الطريقة التي أبلغوا بها عن نتائج التجارب السريرية. لقد كانت طريقة خاطئة وتؤكد وجود مشاكل في التواصل".
وصف خبراء آخرون التدخل العلني للمعهد الوطني الأمريكي للحساسية والأمراض المعدية بالضار للغاية وقالوا: "نشر تصريحات تفيد بوجود شيء غير لائق بشأن الطريقة التي تم بها جمع البيانات يعد تصرفاً غير مسؤول إلى حد بعيد بالنسبة للمعاهد الصحية الوطنية، وبالتالي لا يمكن الوثوق بها. فالأهم هنا هو الطريقة التي تم بها نشر المعلومات بغض النظر عما قيل بالفعل".
وعن رأيه بشأن تلك التصريحات قال بيتر إنغليش الرئيس السابق للجنة طب الصحة العامة التابعة للجمعية الطبية البريطانية: "الأمور ربما كانت سيئة للغاية وأساءت إلى سمعة اللقاح بشكل عام، وهو ما قد يجعل الناس تعتقد بوجود مراوغة بشأن اللقاح الأمر الذي سوف يؤثر على الثقة في لقاح أسترازينيكا وعلى اللقاحات بشكل عام".
يبقى التحدي الرئيسي التالي لأسترازينيكا وهو الحصول على موافقة إدارة الغذاء والدواء على الاستخدام في حالات الطوارئ. فهي تحتاج لأسابيع للحصول على الموافقة ولا يمكن للمسؤولين التنفيذيين في أسترازينيكا اعتقاد أن الأمر سيكون سهلاً، حيث عليهم العمل مع مجلس مراقبة السلامة والبيانات وتقديم بيانات معقدة بالنسبة لأي مطور بين مطوري لقاحات كوفيد في ظل ظهور حالات التخثر والحاجة لتوفير الأدلة الواقعية لتلك الحالات من بين ملايين الأشخاص الذين تم تطعيمهم.
ومن بين التحديات التي واجهتها أسترازينيكا قيام "إميرجنت بايوسوليوشن" إحدى شركات تصنيع اللقاح في الولايات المتحدة نهاية مارس بخطأ تصنيعي فادح، حيث قاموا بخلط المكونات بين لقاح أسترازينيكا ولقاح جونسون أند جونسون ما اضطر إميرجنت إلى اقتصار عملها على تصنيع جرعات جونسون أند جونسون، بينما يعمل المسؤولون الأمريكيون على إيجاد قدرة تصنيعية جديدة لشركة أسترازينيكا.
يشعر العديد من الأشخاص داخل أسترازينيكا بإحباط كبير بسبب النقد الذي تلقوه نتيجة محاولتهم السعي للوصول إلى لقاح غير هادف للربح يمكن أن يساعد في إنهاء الوباء. حيث قال أحد المديرين التنفيذيين في الشهر الماضي عندما سئل عمَّا إذا كانوا سيفعلون ذلك مرة أخرى: "ليس بعد مليون سنة، فالحزن هو ما يسيطر علينا في الوقت الحالي".