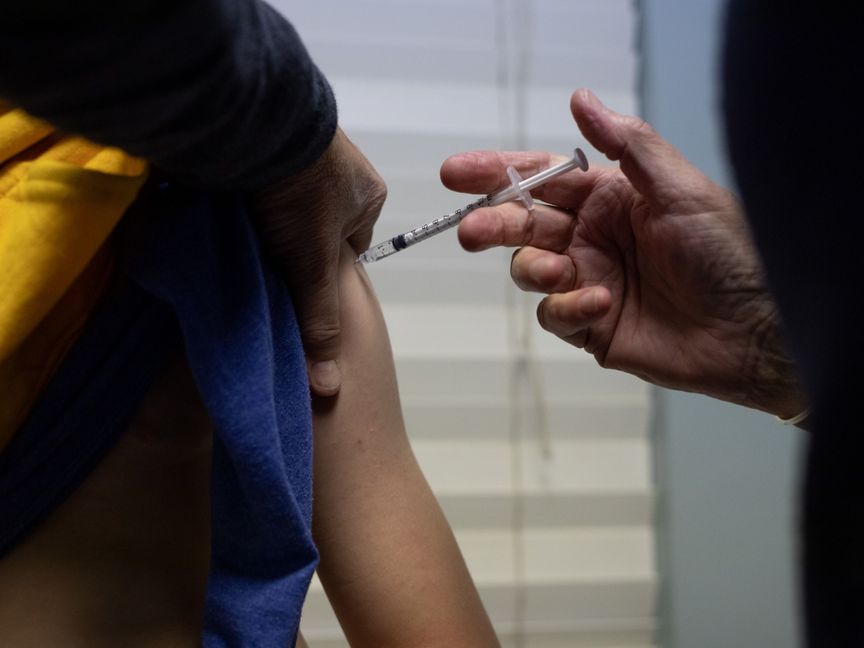
طلبت شركة "فايزر" من الجهات التنظيمية الأمريكية، السماح باستخدام لقاحها المضاد لكورونا في حالات الطوارئ للأطفال دون سن الخامسة، في محاولة منها لتوسيع نطاق الحماية ضد الفيروس لتشمل فئة الصغار في البلاد.
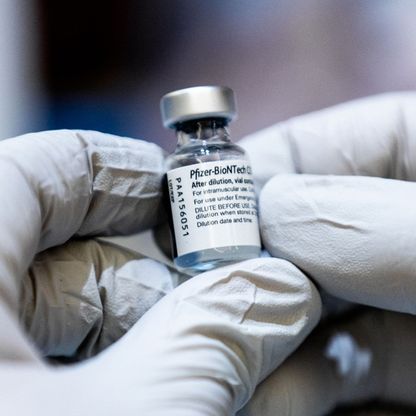
وضعت شركتا فايزر و"بيونتيك" الصيغة النهائية لطلبهما المقدم إلى إدارة الغذاء والدواء الأمريكية للحصول على إذن استخدام طارئ للقاحهما لدى الأطفال بين 6 أشهر و4 أعوام، حيث بدأ الشريكان التقديم في فبراير، بحسب بيان صادر اليوم.
اقرأ أيضاً: "فايزر" تبقي على توقعاتها لمبيعات علاج كورونا في 2022
أعلنت "فايزر" و"بيونتيك" أواخر مايو أن نظام اللقاح ثلاثي الجرعات كان فعَّالاً للغاية وأنه أحدث آثار استجابة مناعية قوية لدى الأطفال دون الخامسة، استناداً إلى نتائج مبكرة من تجربة ستمهد على الأرجح الطريق لتحصين الرضع والأطفال الصغار.
وجد التحليل الأولي أن فعالية اللقاح في وقاية الأطفال الصغار من عدوى كورونا بلغت 80.3%، فلم يكن هناك سوى 10 إصابات بين كافة المشاركين. ستُحدد النتائج النهائية بمجرد إصابة 21 طفلاً مسجلين في الدراسة بالعدوى، بحسب الشركتين.
أطلقت "فايزر" و"بيونتيك" في فبراير استعراضاً متجدداً للبيانات من التجربة التي شملت 1,678 طفلاً دون سن الخامسة. كان نظام اللقاح ثلاثي الجرعات جيداً، وسط وجود موجز أمن مشابه لذلك الخاص بالعقاقير الوهمية، فضلاً عن أن معظم الآثار الجانبية كانت خفيفة أو معتدلة.
طالع أيضاً: دراسة: فاعلية لقاح فايزر المضاد لـ"كورونا" تنخفض بعد 6 أشهر
يتضمن التقديم الكامل للطلب بيانات عن سلامة المنتج وفعاليته وقدرته على تحفيز الاستجابة المناعية. حصل الأطفال دون سن الخامسة على سلسلة مكونة من ثلاث جرعات، كل منها مكون من 3 ميكروغرام، أو 1/10 الكمية المعطاة للبالغين.
مع اكتمال التقديم الآن، سيتحول الانتباه إلى اجتماع اللجنة الاستشارية لإدارة الغذاء والدواء المقرر في 15 يونيو، حيث ستجتمع لجنة الخبراء لمناقشة مخاطر وفوائد لقاحات "فايزر - بيونتيك" و"موديرنا" لدى الأطفال الصغار وتقديم توصية للجهات التنظيمية الأمريكية بشأن ما إذا كان ينبغي استخدام اللقاح في حالات الطوارئ أم لا.
قالت "فايزر" إن الشركات تخطط أيضاً لتقديم البيانات إلى وكالة الأدوية الأوروبية والجهات التنظيمية الأخرى حول العالم.